近日,上海交通大学生命科学技术学院、微生物代谢国家重点实验室白林泉科研团队深入解析了抗糖尿病药物阿卡波糖生物合成机制,通过有效的代谢工程策略进一步提高了阿卡波糖产量。相关研究成果以“A severe leakage of intermediates to shunt products in acarbose biosynthesis”为题发表于Nature Communications杂志上。上海交通大学博士研究生赵芹芹为论文第一作者,白林泉教授为通讯作者,该文作者还包括邓子新院士、塔里木大学张利莉教授等。
阿卡波糖是α-糖苷酶抑制剂类天然产物,在临床上作为一线药物被广泛用于2型糖尿病的治疗,需求量大,年市场销售额超过70亿人民币。在工业上,阿卡波糖主要通过游动放线菌发酵生产。由于生物合成路径复杂及产生多种副产物和结构类似物,导致其产量较低和后提取工艺十分繁琐。因此,构建高效的生产菌株,提高工业化生产水平,是目前亟待解决的关键问题。然而,由于大部分生物合成途径尚不清楚,严重阻碍了通过代谢工程改造对产量的大幅提升。
在这项研究中,作者在发酵液中鉴定出两种大量积累的来自阿卡波糖合成途径的分流产物。通过对这些分流产物及其形成方式的系统深入研究,明确了环醇脱水酶AcbL和NADPH依赖性氧化还原酶AcbN的功能,修正了阿卡波糖的生物合成途径。同时通过比较转录组分析,发现氨基脱氧己糖部分的低效生物合成是引起分流产物形成的主要原因之一。在此基础上,作者以“开源截流”策略为指导,采用多种代谢工程与合成生物学手段,一方面通过多基因敲除最大限度地减少分流产物的积累,另一方面通过异源高效氨基脱氧己糖合成基因的引入来提高其合成能力,促进C7-环醇中间体的有效利用,最终使阿卡波糖产量提高了1.2倍,达到7.4 g/L。
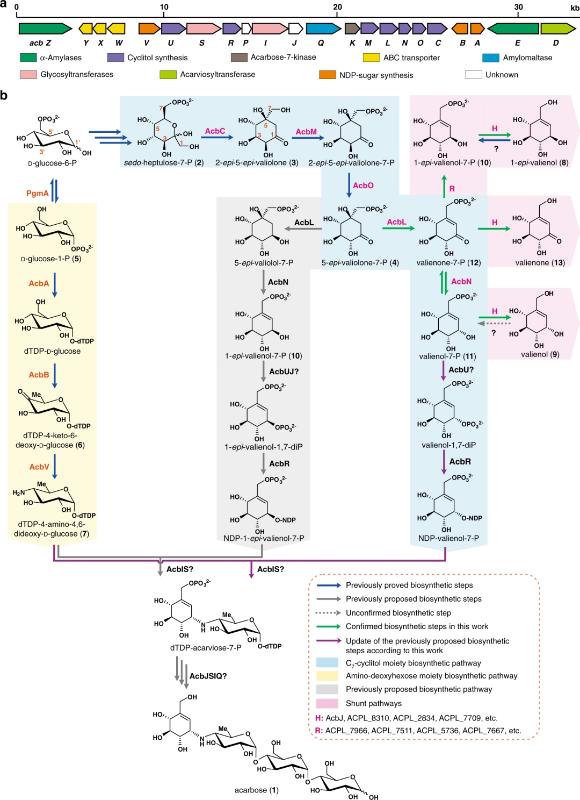
这项研究打破了近20年来阿卡波糖生物合成机制研究的沉寂,也是首次采用分子生物学与合成生物学手段对其产生菌的系统、有效改造,为阿卡波糖的定向高产和提升该领域的国际竞争力奠定了坚实基础。这项研究不但强调了分流产物在微生物药物合成与产量提高中的重要性,还揭示了多样的初级代谢与次级代谢的交叉对话,可以更加有效的指导微生物药物的高产改造。该项研究展现了邓子新院士团队在井冈霉素、阿卡波糖等氨基环醇类天然产物方面的长期研究积累,高效的遗传操作系统、井冈霉素多种代谢中间体和关键酶、氨基环醇合成机制假说等都是取得本项研究突破的关键。
该研究获得国家自然科学基金委重点项目和联合基金项目、国家重点研发计划项目、上海市科委基础研究项目等的支持。(上交新闻网)
标签: 上海交通大学